
Közel 200 évvel azután, hogy Michael Faraday felfedezte a molekulát, a kutatók végül felfedezték a benzol összetett elektronikus szerkezetét.
Ez nemcsak az 1930-as évek óta tomboló vitát oldja meg, hanem fontos következményekkel jár az optoelektronikus anyagok jövőbeni fejlődése szempontjából, amelyek közül sok benzolon alapszik.
A benzol atomszerkezete meglehetősen jól érthető. Ez egy gyűrű, amely hat szénatomból és hat hidrogénatomból áll, mindegyik szénatomhoz egy.
Ez rendkívül nehézzé válik, ha egy molekula 42 elektronját vesszük figyelembe.
“A benzol elektronjait leíró matematikai függvény 126 dimenziós” – mondta Timothy Schmidt vegyész, az ARC Exciton Science Kiválósági Központjának és az ausztráliai UNSW-nek.
'Ez azt jelenti, hogy 126 koordináta függvénye, három a 42 elektron mindegyikéhez. Az elektronok nem függetlenek, ezért ezt nem tudjuk lebontani 42 független 3D funkcióra.
A gép válaszát az emberek nem könnyen értelmezik, és ki kellett találnunk a választ.
Ez tehát azt jelenti, hogy a benzol elektronikus szerkezetének matematikai leírásakor 126 mérést kell figyelembe venni. Ahogy el lehet képzelni, ez nem könnyű dolog. Valójában e bonyolultság miatt a szerkezet feltárása ilyen hosszú ideig probléma maradt, és vita alakult ki a benzol elektronok viselkedéséről.
Kétféle gondolkodásmód létezik: a benzol a lokalizált elektronokkal végzett valens kötések elméletét követi; vagy molekuláris pályaelmélet delokalizált elektronokkal. A probléma az, hogy egyikük sem tűnik igaznak.
“Az elektronikus szerkezet pályákra való értelmezése figyelmen kívül hagyja, hogy a hullámfüggvény antiszimmetrikus ugyanazon pörgetések cseréjénél” – írták a kutatók cikkükben. “Ráadásul a molekuláris pályák nem adnak intuitív leírást az elektronkorrelációról.”
A csapat munkája egy nemrégiben kifejlesztett technikán alapult. A Voronoi Metropolis dinamikus mintavételének hívják, és algoritmikus megközelítést alkalmaz a többelektronikus rendszer hullámfüggvényeinek vizualizálására.
Ez egy Voronoi-diagramban az elektronikus méreteket külön csempékre osztja, ahol mindegyik lap megfelel az elektronikus koordinátáknak, lehetővé téve a csapat számára, hogy megjelenítse mind a 126 dimenzió hullámfüggvényét.
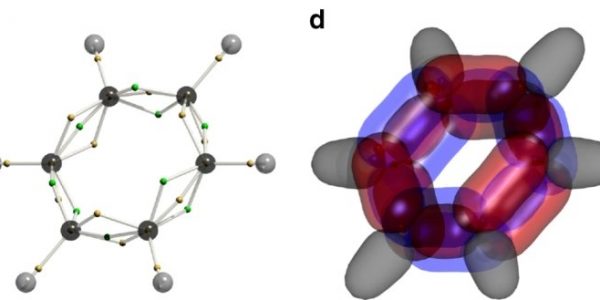
Egy molekula keresztmetszete. (Liu és mtsai. Nature Communications, 2020)
És találtak valami furcsát.
“Az úgynevezett kettős kötésekkel rendelkező elektronok a forgási sebesség növekedésével, ahol az egyszeres kötésű elektronok a forgási sebesség csökkenésével és fordítva” – mondta Schmidt. “A vegyészek nem így gondolkodnak a benzolról.”
Ennek eredményeként az elektronok elkerülik egymást, amikor ez hasznos, csökkentve a molekula energiáját és stabilabbá téve azt.
“Alapvetően összefogja a kémiai gondolkodást, megmutatva, hogyan áll össze a benzol leírására használt két uralkodó paradigma” – mondta.
De azt is megmutatjuk, hogyan tesztelhetjük az úgynevezett elektronkorrelációt – hogyan kerülik egymást az elektronok. Ezt szinte mindig minőségileg figyelmen kívül hagyják, és csak számításokhoz használják, ahol csak energiát használnak fel, nem pedig az elektronikus viselkedést. ”
A tanulmány a Nature Communications folyóiratban jelent meg.






